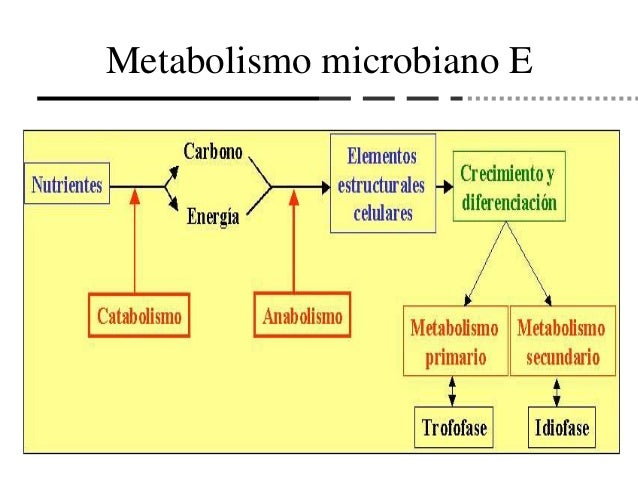
Metabolismo productor de energía
En los seres vivos, la utilización de la energía potencial contenida en los nutrientes se produce por reacciones de oxidación reducción. Químicamente la oxidación esta definida por la pérdida de electrones y, la reducción por la ganancia de los mismos. En bioquímica, estas reacciones frecuentemente incluyen también la transferencia de átomos enteros de hidrógeno, por lo tanto se conocen con el nombre de reacciones de deshidrogenación. En las reacciones de este tipo hay sustancias que ceden electrones (dadoras) y otras que los aceptan (aceptoras). En las bacterias de interés médico los sistemas de oxidación reducción transforman la energía química de los nutrientes en una forma biológicamente útil; dichos procesos incluyen la fermentación y la respiración. En la primera, tanto la molécula dadora como la aceptora de electrones, son compuestos orgánicos. En cambio, en la respiración hay un aceptor final exógeno, que cuando es el oxígeno se denomina respiración aerobia y cuando es un compuesto inorgánico, respiración anaerobia.
Fermentación
En ésta los electrones pasan del dador, un intermediario formado durante la degradación del substrato, hacia un aceptor constituido por algún otro intermediario orgánico también generado durante el catabolismo del substrato inicial. Por lo tanto, este proceso de oxidación reducción no requiere el aporte exógeno de un aceptor final de electrones. Aunque hay distintos tipos de fermentaciones, todas llevan a una oxidación parcial de los átomos de carbono del substrato inicial y liberan, por lo tanto una pequeña parte de la energía potencial contenida
- Fermentación alcohólica Es el tipo de fermentación más antigua que se conoce. Produce etanol a partir de glucosa. Aunque ciertas bacterias producen alcohol, éste es elaborado por otras vías.
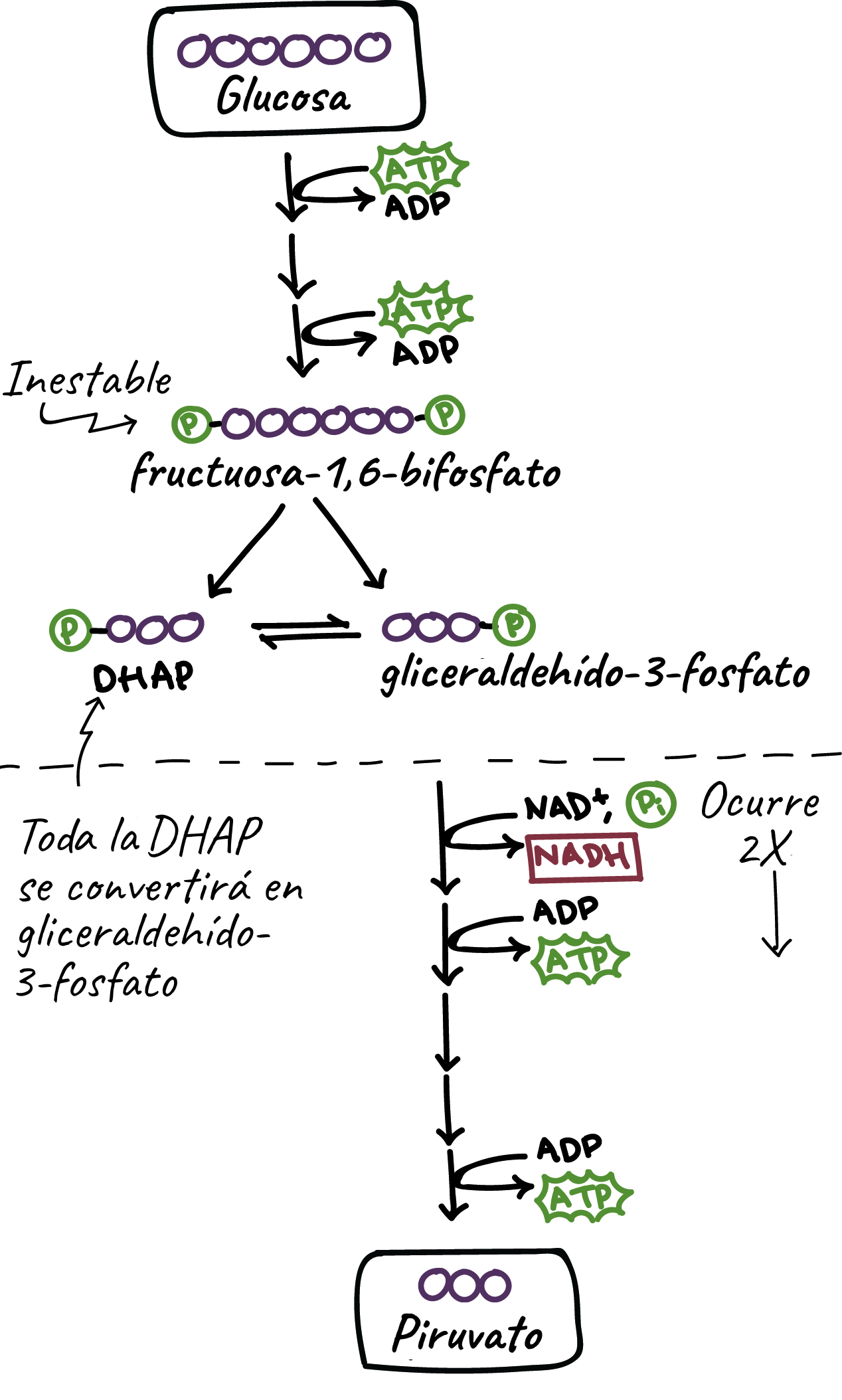
- Fermentación homoláctica Todos los miembros del género Streptococcus, Pediococcus y muchas especies de Lactobacillus fermentan la glucosa fundamentalmente a ácido láctico con poca acumulación de otros productos finales. En esta reacción el piruvato se reduce a ácido láctico por acción de la enzima láctico deshidrogenasa, actuando el NADH como dador de electrones. Esto ocurre en la tercer etapa de la vía glucolítica.
- Fermentación heteroláctica En este tipo de fermentación solo la mitad de la glucosa se convierte en ácido láctico, el resto se transforma en una mezcla de anhídrido carbónico (CO2 ), ácido fórmico, ácido acético, etc. En esta fermentación se emplea fundamentalmente la vía de las pentosas y se produce en las bacterias del género Leuconostoc y Lactobacillus.
- Fermentación del ácido propiónico Es característica de algunas bacterias anaerobias como el Propionibacterium (bacilo grampositivo, no esporulado). Este tipo de fermentación tiene la ventaja de que genera una molécula más de ATP. Fermentación ácido mixta Es característica de la mayoría de las enterobacterias. Bacterias como Shigella, Salmonella y E. coli fermentan las hexosas a través del piruvato a ácido láctico, ácido acético, ácido succínico y ácido fórmico.
- Fermentación de butanodiol Varias bacterias como Enterobacter, Serratia y Bacillus producen 2,3-butanodiol durante la fermentación de la glucosa. Este deriva de la condensación de dos moléculas de piruvato en una molécula neutra de acetoína que luego es reducida a 2,3-butanodiol.
- Fermentación del ácido butírico Se ve en bacterias del género Clostridium (bacilo grampositivo, anaerobio y esporulado). Si bien hasta ahora nos hemos referido solo a la fermentación de hidratos de carbono como procedimiento para obtener energía, debemos destacar que otros compuestos orgánicos pueden ser fermentados, por ejemplo: aminoácidos (alanina, glicina). En Clostridium proteolíticos, la fermentación de aminoácidos más característica es la reacción de Stickland.
Respiración
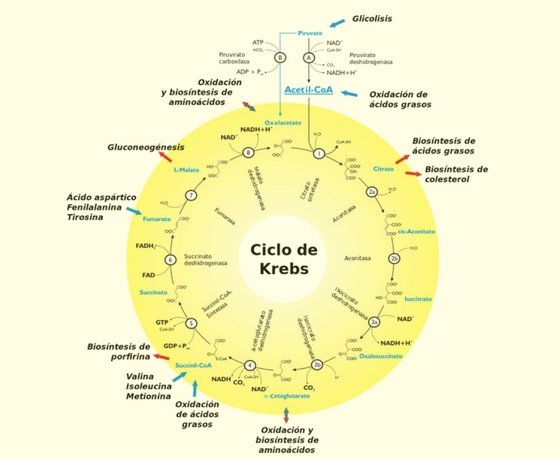
Es el proceso por el cual un substrato es oxidado completamente a CO2 y agua, con participación de una cadena de electrones ubicada en la membrana plasmática, en la cual el aceptor final es el oxígeno molecular u otro compuesto inorgánico (nitratos, sulfatos, anhidrido carbónico, etc.)–anaerobia–. Los primeros pasos en la respiración de la glucosa son idénticos a los de la glucólisis, pero mientras en esta última el piruvato es convertido en productos finales de la fermentación (ácido láctico, ácido propiónico, etc.), en la respiración es oxidado completamente a CO2 mediante el ciclo de Krebs
Por cada molécula de piruvato oxidada en este ciclo, se generan tres moléculas de CO2 . Al igual que en la fermentación, los electrones generados en el ciclo de Krebs, pasan a coenzimas que tienen NAD. Sin embargo, en la respiración aerobia, los electrones del NADH son transferidos al oxígeno para regenerar NAD a través de un sistema transportador, en lugar de cederlos al piruvato.
Sistemas Transportadores de Electrones y Generación de Trifosfato de Adenosina.
Estos sistemas están compuestos por transportadores (carriers) de electrones, asociados a la membrana plasmática y tienen dos funciones básicas: aceptar electrones de un donador y cederlos a un aceptor y conservar energía liberada durante ese transporte en forma de ATP por fosforilación oxidativa. Existen varios tipos de enzimas de oxidación reducción y proteínas transportadoras de electrones, entre los que se destacan las NAD-deshidrogenasas, las flavoproteínas y los citocromos. Las flavoproteínas contienen un derivado de la riboflavina como grupo prostético que se reduce y se oxida alternativamente. La riboflavina, conocida como vitamina B2, es necesaria como factor de crecimiento por algunas bacterias. Los citocromos son proteínas que tienen anillos porfirínicos con hierro y también se oxidan y se reducen alternativamente. Hay diferentes tipos de citocromos que se distinguen por sus potenciales de reducción. Se los designa con letras a, b, c, etc. También están las quinonas, sustancias liposolubles relacionadas con la vitamina K, que participan en el transporte de electrones. Para entender como se genera el ATP durante el transporte de electrones, debemos recodar su orientación con respecto a la membrana plasmática de la célula bacteriana. La cadena está ubicada como ya dijimos en la membrana plasmática, de tal modo que durante el proceso de transporte hay una separación física entre protones y electrones. Los protones quedan fuera de la célula, mientras que los electrones quedan dentro de ésta; en consecuencia se genera un gradiente de pH y un potencial eléctrico a través de la membrana plasmática, estando el lado externo ácido y cargado positivamente y el interno alcalino y cargado negativamente. A pesar de su tamaño pequeño, ni los hidrogeniones, ni los hidróxidos atraviesan libremente la membrana; por lo tanto, el equilibrio no puede establecerse espontáneamente. Dicho estado energético de la membrana plasmática, similar a una batería, puede ser usado por la célula para realizar un trabajo útil, por ejemplo, movilidad o síntesis de ATP. Para la síntesis de ATP un componente fundamental del proceso es una ATPasa de membrana; enzima que cataliza la reacción reversible entre difosfato de adenosina (ADP) y ATP. Operando en una dirección y usando el gradiente de protones generado durante el transporte, dicha enzima cataliza la formación de ATP a partir de ADP y fosfato inorgánico. Existe una variedad de agentes químicos llamados desacopladores que inhiben la síntesis de ATP durante el transporte de electrones sin alterar el propio proceso de transporte. Ejemplos de estos agentes son el dicumarol y el dinitrofenol. Son sustancias liposolubles que impiden la formación del gradiente de pH y el eléctrico, favoreciendo el pasaje de protones a través de la membrana; de este modo inhiben la síntesis de ATP. La polimixina B (un antibiótico) se adhiere específicamente a la superficie externa de la membrana, alterando su estructura y propiedades osmóticas. Se produce entonces la pérdida de metabolitos y la inhibición de algunos procesos bioquímicos que tienen lugar a ese nivel, como el transporte de electrones y la síntesis de ATP, entre otros. Otras sustancias, por ejemplo: cianuro o azida de sodio, bloquean el propio sistema de transporte y se denominan inhibidores. Tanto los desacopladores como los inhibidores son venenos celulares que actúan en células eucariotas y procariotas.
Balance Energético de la Respiración
El resultado neto de las reacciones del ciclo de Krebs es la oxidación completa del piruvato a CO2 con formación de cuatro moléculas de NADH y una de dinucleótido de flavinadenina (FADH). El NADH y el FADH pueden ser oxidados nuevamente por el sistema transportador de electrones. Un total de 15 moléculas de ATP son sintetizadas en cada vuelta del ciclo, por lo tanto, dado que cada molécula de glucosa rinde dos de piruvato, 30 moléculas de ATP son sintetizadas por cada molécula de glucosa que entra al ciclo de Krebs
Esto, sumado a las seis moléculas de la reoxidación del NADH y las dos del vía glucolítica, da un total de 38 moléculas de ATP por molécula de glucosa respirada. Además de sus funciones como mecanismo generador de energía, el ciclo de Krebs sirve como productor de metabolitos claves para la biosíntesis. La reducción del oxígeno forma radicales libres que son muy tóxicos para la bacteria. Entre los más importantes se encuentra el superóxido. Éste es eliminado por las bacterias aerobias y tolerantes del oxígeno, por la enzima superoxidodismutasa que cataliza la formación de peróxido de hidrógeno, también tóxico. El peróxido de hidrogeno es degradado por enzimas como catalasa y la peroxidasa, a oxígeno molecular y agua. Estas enzimas están ausentes en las bacterias anaerobias estrictas, explicando en parte la susceptibilidad que tienen al oxígeno. En las bacterias aerobias obligadas, el oxígeno es el aceptor final de electrones. Sin embargo, las bacterias anaerobias facultativas pueden usar, en ausencia de oxígeno, otros compuestos inorgánicos como aceptores finales de electrones, por ejemplo: nitrato, fumarato, sulfato, etc.
Regulación del Metabolismo.
Cada reacción metabólica está regulada no solo con respecto a otras reacciones, sino también con respecto a la concentración de nutrientes en el medio. La regulación se realiza a diferentes niveles: en la actividad enzimática y en la síntesis de las enzimas. En la primera, regulación de la actividad enzimática, se produce: activación de enzimas alostéricas, inhibición por retroalimentación, activación alostérica y cooperatividad. La inducción enzimática y la represión por productos finales, son mecanismos de regulación de la síntesis de enzimas. En las bacterias anaerobias facultativas la fermentación (como única vía de producción de energía) es bloqueada en presencia de oxígeno, asegurando que el suministro de energía se produzca por respiración, que consume menos glucosa y acumula menos lactato. En este fenómeno denominado efecto Pasteur, la enzima fosfofructoquinasa es activada o inhibida según la relación entre el ATP y el ADP, regulando así el consumo de glucosa. Este es un ejemplo de regulación de la actividad enzimática por una enzima alostérica. El ejemplo clásico de regulación de la síntesis de enzimas lo constituye el operón lactosa. Hay tres enzimas que participan en la utilización de la lactosa (ß-galactosidasa, galactósido permeasa y galactósido transacetilasa), las cuales tienen un promotor único. En ausencia de lactosa, la transcripción para estas enzimas está bloqueada por un represor que se une al promotor inhibiendo la acción de la ARN polimerasa. Cuando se agrega lactosa al medio, ésta se une al represor, bloqueando de este modo su unión al promotor y permitiendo la acción de la ARN polimerasa y la síntesis de las tres enzimas anteriormente mencionadas.






No hay comentarios.:
Publicar un comentario